Représentativité et réactivité du système de surveillance de la Fièvre Jaune au Togo, 2004-2014
Representativeness and responsiveness of the Yellow Fever surveillance system in Togo, 2004-2014
Wemboo Afiwa Halatoko1, Akouda Patasse2,3, Simon Hamadi Assane4, Aboukerim Naba Mouchedou5, Agballa Mébinesso Tchalla6, Yao Layibo1, 3, Adodo Yao Sadji1, Adjaho Koba1, Koffi Akolly1, Christelle Somtinda Nikiéma7, Bernard Sawadogo8, Simon Nyuvura Antara8, Kossi Badziklou1
1Institut National d´Hygiène de Lomé, Togo, 2Centre Hospitalier Universitaire Sylvanus Olympio, Lomé, Togo, 3Université de Lomé Faculté des Sciences de la Santé Lomé, Togo, 4Direction de la Lutte contre la Maladie Lomé, Togo, 5Direction de la Santé Communautaire: Lomé, Togo, 6Direction Pré-fectorale de la Santé Haho, Togo, 7Division de la Surveillance Intégrée, de la Riposte et des Urgences Sanitaires, Lomé, Togo, 8African Field Epidemiology Network Kampala (AFENET)
&Auteur correspondant
Wemboo Afiwa Halatoko, Institut National d´Hygiène de Lomé, Togo.
hjacky78@yahoo.fr
Introduction:
Peu d’informations sont disponibles sur le système de surveillance de la fièvre jaune au Togo. L’objectif est d’évaluer la simplicité, la représentativité et la réactivité de ce système.
Méthodes:
Une étude transversale descriptive a été menée de 2015 à 2016 à l’Institut Na-tional d’Hygiène (INH) qui est le Laboratoire National de Référence (LNR) pour les maladies à po-tentiel épidémique du Togo. La base de données de 2004-2014 de la fièvre jaune- rougeole -rubéole du LNR et le guide de surveillance intégrée des maladies et riposte, le guide d’évaluation des systèmes de surveillance de Centers for Disease Control and Prevention (CDC) ont été utilisés. Les médianes, intervalles interquartiles et les proportions ont été calculés avec Epi Info 7 et Excel 2003.
Résultats:
Un cas suspect de fièvre jaune nécessite une confirmation biologique qui se fait à plusieurs niveaux. Le système est représentatif de tous les districts, toutes les années et de toutes les populations du Togo. Un total de 3054 de cas suspects a été notifié dont 32 cas probables et 12 cas confirmés, par-mi lesquels, 8 étaient des hommes.
Environs 93,01 % (2833) des cas suspects ont été prélevés dans les 14 jours suivants le début des symp-tômes, 28,39% (866) des échantillons ont été acheminés dans les 72 heures et 77,95% des résultats rendus dans les 7 jours rendant le système peu réactif.
Conclusion:
Le système de surveillance de la fièvre jaune au Togo est représentatif, complexe et peu réactif. Il s’avère nécessaire de mettre en place un système de convoyage rapide des échantillons.
English abstract
Introduction: Little information is available on yellow fever surveillance system in Togo. The simplicity, representativeness and responsiveness of this system were assessed.
Material and methods: It was a descriptive cross-sectional study conducted from October 2015 to February 2016 at the Institut National d’Hygiène, the National Reference Laboratory (NRL) for epidemic prone diseases of Togo. We used the yellow fever-measles-rubella database, the integrated dis-ease surveillance and response guideline and the Centers for Disease Control and Prevention (CDC) guidelines for surveillance system evaluation. Medians, interquartile intervals and proportions were calculated and presented in tables and figures with Excel 2003 and Epi Info 7.
Results: A yellow fever case must be confirmed at several reference levels making yellow fever surveillance complex. This surveillance system is representative of all districts, all years and all populations of Togo. A total of 3054 suspected cases were reported, including 32 probable cases and 12 confirmed cases. Of the confirmed cases, 08 were men. About 93.01% (2833) of the suspected cases samples were taken within 14 days after the symptoms onset, 28,39% (866) of samples were transported within 72 hours and 77, 95% of the results were available within 7 days, making the system unresponsive.
Conclusion: The yellow fever surveillance system in Togo is representative, complex, and unresponsive due to the long delay in transporting samples to the NRL. A rapid sample conveying system is recommended.
Key words: yellow fever, representativeness, complexity, responsiveness, Togo
Introduction

La fièvre jaune est une fièvre hémorragique transmise par la piqûre de moustique infecté par un arbo-virus de la famille des flavivirus. Le moustique en cause est du genre Aedes et se re-produit très facilement dans tous les types de gîtes artificiels domestiques et péri domestiques tels que les vases, les réservoirs d´eau, les boîtes de conserve, les noix de coco cassées, les pneus usagés et les égouts [1]
L´évolution de la maladie peut se faire vers une guérison spontanée ou vers la mort dans 50 à 80% des cas dans les formes graves [
2]
La fièvre jaune est endémique dans la zone tropicale en Afrique et en Amérique du Sud.
L´Organisation mondiale de santé (OMS) estime entre 84 000-170 000 le nombre de cas sévères et entre 29 000-60 000 le nombre de décès liés à la fièvre jaune dans le monde par année [
3,
4]. La majo-rité des cas survienent dans 34 pays d´Afrique Sub-Sahariens qui sont endémiques où 500 millions de personnes sont exposées [
4,
5]
Le Togo du fait de sa position géographique est un pays à risque de fièvre jaune et avait bénéficié de plusieurs campagnes de vaccination de masse contre la fièvre jaune dont la dernière en date remonte à 2007 [
6].
Le contrôle de la fièvre jaune est l´une des priorités sanitaires au Togo et se fait à travers une surveil-lance épidémiologique fondée sur l´identification des cas depuis 2002 comme le recommande l´OMS [
7]
Le vaccin antiamaril a été introduit dans le programme élargi de vaccination en janvier 2005 au Togo.
Le système de surveillance épidémiologique de la fièvre jaune au Togo permet de confirmer les cas, de détecter des épidémies et de mener des campagnes de vaccination de riposte.
L´évaluation périodique des systèmes de surveillance est nécessaire pour s´assurer que le problème de santé publique est suivi de façon efficiente et efficace [
8]. Cependant il existe peu d´informations sur les performances du système de surveillance de la fièvre jaune du Togo qui n´a jusqu´alors fait l´objet d´aucune évaluation documentée. Cette étude contribuera à éclairer les acteurs de la lutte contre la fièvre jaune et dans la formulation de politiques de santé.
L´objectif de cette étude est d´évaluer la simplicité, la représentativité et la réactivité du système de surveillance épidémiologique de la fièvre jaune de 2004 à 2014 au Togo.
Méthodes


Cadre d´étude
Le Togo, pays de 56000 km2, est compris entre la République du Ghana à l´ouest, la République du Bénin à l´est, la République du Burkina Faso au nord et l´océan atlantique au sud.
Deux climats prévalent au Togo : l´un subéquatorial et l´autre tropical humide. Le climat équatorial règne sur la moitié sud du pays et est caractérisé par deux saisons sèches (de novembre à mars et de juillet à août), et deux saisons pluvieuses (de mars à juillet et de septembre à octobre). La moitié nord du pays est couverte par le climat tropical humide, qui se caractérise par une seule saison des pluies (de mai à octobre) et une saison sèche (de novembre à avril) avec des températures très élevées surtout dans le district de l´Oti.
La pyramide sanitaire du Togo est à trois niveaux:
- le niveau central qui est le niveau de conception et d´orientation, est composé du cabinet du Ministre, de la direction générale, de 5 directions centrales avec 15 divisions et 39 services;
- le niveau intermédiaire ou niveau d´appui technique est constitué de 6 directions régionales;
- le niveau périphérique ou local qui est le niveau opérationnel, est composé de 40 districts sanitaires.
I´Institut National d´Hygiène (INH) qui est au niveau central de la pyramide sanitaire du Togo a pour missions la réalisation des analyses de biologie médicale, le contrôle de la qualité microbiologique et physico-chimique de l´eau et des aliments, les vaccinations des voyageurs conformément au Règle-ment Sanitaire International, les contrôles aux postes frontières et la participation à la surveillance des maladies à potentiel épidémique en collaboration avec la Division de la Surveillance Intégrée des Ma-ladies et Urgences Sanitaires avec l´appui des partenaires.
L´INH est le laboratoire national de référence pour la confirmation des maladies à potentiel épidé-mique (MPE) : méningites, cholera, shigellose, rougeole, rubéole, grippe, fièvre jaune, et autres fièvres virales hémorragiques. Il forme avec les laboratoires des districts et des régions du Togo le Réseau National des Laboratoires pour la confirmation des MPE. Tous les échantillons de cas suspects de MPE d´origine virale sont directement convoyés à l´INH celle d´origine bactérienne font l´objet d´examens directs et ou de culture au niveau des laboratoires des districts et régions avant leur trans-fert à l´INH pour la culture ou et la biologie moléculaire. Une base nationale des données épidémiolo-giques et biologiques de la surveillance de la fièvre jaune, rougeole et rubéole est aussi disponible à l´INH.
Type et période d´étude
Il s´est agi d´une étude transversale descriptive basée sur les données de surveillance de la fièvre jaune.
Population d´étude et échantillonnage
Tous les cas suspects de fièvre jaune du Togo ayant fait l´objet d´un prélèvement sanguin entre 2004 et 2014 et dont les données étaient disponibles dans la base de données de l´INH ont été inclus.
Définitions opérationnelles
Représentativité: c´est la capacité d´un système à décrire les cas selon le temps, le lieu et les personnes [
8].
Simplicité: se réfère à la fois à sa structure et à la facilité de l´utilisation d'un système de surveillance [
8].
Réactivité d´un système de surveillance épidémiologique c´est le délai (en jours) entre les étapes du système de surveillance ou sa rapidité à riposter en cas d´épidémie [
8]. Dans cette étude nous nous sommes appesantis sur les délais pour évaluer la réactivité du système de surveillance de la fièvre jaune.
Les délais en jours ont été estimés :
- Délai d´acheminement des échantillons au LNR : c´est la durée qui s´écoule entre le prélève-ment lors de l´investigation et son arrivée au LNR ;
-
- Délai de rendu des résultats par le LNR : c´est la durée qui s´écoule entre l´arrivée du prélè-vement au laboratoire et sa manipulation;
-
- Délai de confirmation biologique est le temps écoulé entre la notification et le rendu des résul-tats du laboratoire à la division de la surveillance épidémiologique.
-
La représentativité du système de surveillance a été appréciée à partir des capacités du système à dé-crire les cas en termes de temps lieux et personnes et la simplicité en analysant son organisation, la définition des cas et les méthodes de confirmation des cas.
Collecte des données
Une revue du guide de surveillance intégrée des maladies et riposte du Togo a été faite et une extrac-tion des données de 2004-2014 de la fièvre jaune à partir de la base de données commune fièvre jaune-rougeole-rubéole du LNR du Togo été faite à l´aide d´un fichier Excel.
Le guide d´évaluation d´un système de surveillance de CDC [
8] a été utilisé pour la présente étude.
Variables d´étude
L´âge, le sexe, le district de résidence, la date de notification des cas, la date d´investigation et de pré-lèvement des cas, la date de réception du prélèvement au laboratoire, la date de confirmation de cas par le laboratoire national de référence puis par le laboratoire régional de référence, les résultats d´analyse de laboratoire ainsi que leur date communication ont été des variables étudiées.
Analyse et traitement des données
Les données ont été saisies et analysées avec le logiciel Epi Info 7 et Excel 2003. Les doublons ont été supprimés et les données manquantes ont été complétées à partir des registres disponibles au LNR. Les variables quantitatives ont été résumées selon leurs médianes et leurs intervalles interquartiles (IIQ) et les variables qualitatives selon leurs proportions.
Considérations éthiques
Le protocole a été approuvé par la direction de coordination du Master d´Epidémiologie de terrain de l´Université Ouaga 1 Pr. Joseph Ki-Zerbo. La consultation de la base de données a été précédée par un accord de principe des autorités sanitaires du Togo. L´anonymat des patients de la base de données a été assuré.
Résultats


Description du système de surveillance de la fièvre jaune au Togo
La surveillance de la fièvre jaune s´inscrit dans le cadre des activités de surveillance intégrée des mala-dies et de la riposte (SIMR). C´est une surveillance au cas par cas.
Au niveau central la coordination de la surveillance est assurée par la Division de la Surveillance Inté-grée de la Riposte et des Urgences Sanitaires.
Au niveau régional et district, la coordination des activités de surveillance est assurée par les direc-teurs régionaux et préfectoraux de la santé. Les points focaux (PF) de surveillance au niveau district et région sont chargés de la compilation, de l´analyse et de la transmission des données au niveau central avec une périodicité hebdomadaire.
Pour le système d´alerte précoce, au niveau périphérique, la collecte et la transmission des rapports de surveillance se font à travers les réseaux de surveillance épidémiologique. Un réseau est un ensemble d´Unité de Soins Périphériques situées sur un même circuit de collecte de l´information épidémiolo-gique dans un même district.
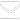
Toute personne suspecte de fièvre jaune fait l´objet d´une investigation et d´un prélèvement de sang veineux pour le diagnostic au laboratoire. Les laboratoires des districts conditionnent les prélèvements dans un système de triple emballage. Les sérums sont convoyés par les PF ou les responsables des formations sanitaires des districts ou régions à l´INH pour un premier test puis les échantillons posi-tifs, probables et 10% des négatifs sont convoyés à Dakar pour d´autres tests. La
Figure 1 illustre le processus de confirmation biologique d´un cas suspect de fièvre jaune.
Objectifs de la surveillance de la fièvre jaune au Togo
Les objectifs de la surveillance de la fièvre jaune du Togo étaient de:
- Détecter et confirmer précocement les cas et les épidémies de fièvre jaune afin d´entreprendre les mesures de riposte pour limiter l´extension de l´épidémie;
- Identifier les populations affectées et celles à risque;
- Suivre l´épidémiologie de la maladie et l´impact des mesures de lutte;
- Soutenir la recherche opérationnelle et l´innovation.
Simplicité du système de surveillance de la fièvre jaune au Togo
Les définitions de cas utilisées étaient celles du Guide SIMR Togo [
9].
Un cas suspect est une personne vivant au Togo et présentant une fièvre brusque avec l´apparition d´une jaunisse dans les 14 jours qui suivent le début des signes.
Un cas probable est une personne répondant à la définition de cas suspect avec l´un des signes sui-vants:
- Un lien épidémiologique avec un cas confirmé au cours d´une épidémie;
- La présence d´IgM dirigés contre la fièvre jaune en absence d´une immunisation contre la fièvre jaune dans les 30 jours avant le début de la maladie ;
- Une histologie hépatique positive en post mortem.
Un cas confirmé est une personne chez qui l´une des observations suivantes est faite en dehors d´une immunisation dans les 30 jours précédents:
- Une détection d´IgM spécifiques de la fièvre jaune;
- Une augmentation de la concentration d´IgM de l´ordre de 4 fois entre la phase aiguë et celle de la phase de convalescence;
- Une détection d´anticorps spécifiques neutralisants.
La confirmation des cas suspects de fièvre jaune passe par plusieurs tests biologiques.
L´analyse sérologique est effectuée à l´INH pour la recherche des anticorps anti amaril type IgM.
La présence d´immunoglobulines M (IgM) de la fièvre jaune ne permet pas d´affirmer que le cas est réellement dû à la fièvre jaune, car l´éventualité d´une réaction croisée survenant par suite d´une expo-sition récente à d´autres
flavivirus doit être écartée par des analyses complémentaires. Le dia-gnostic de confirmation est fait par le laboratoire régional de référence (LRR) à Dakar par un test ELISA, une PCR puis un test de séroneutralisation virale.
La définition de cas de fièvre jaune n´est pas simple et la confirmation au laboratoire se fait à deux niveaux. Aussi l´interprétation des résultats de laboratoire n´est pas facile ce qui rend ce système com-plexe.
Représentativité du système de surveillance de la fièvre jaune du Togo
Le système de surveillance de la fièvre jaune a permis de notifier des cas suspects sur toute l´étendue du territoire togolais et de détecter des épidémies. Tous les cas suspects quel que soit l´âge ou le sexe sont susceptibles d´être détectés par le système de surveillance de la fièvre jaune tel qu´organisé au Togo.
Notification des cas de la fièvre jaune au Togo
Du 1er janvier 2004 au 31 décembre 2014, 3054 cas suspects ont été notifiés et prélevés.
Entre 2005 à 2007 il n´y a pas eu d´échantillon de cas suspects manipulés au laboratoire national de référence. Sur l´ensemble de ces cas suspects notifiés, il y avait 33 (10,81%) cas probables dont 12 (0,39%) cas confirmés.
Un total de 45 échantillons dont 33 probables ont été envoyés au laboratoire régional de Dakar pour confirmation, 12 cas ont été confirmés positifs.
La plupart des districts sanitaires du Togo 36 sur 40 (90%) avait rapporté au moins un cas suspect par an.
Caractéristiques des cas
Cas suspects
Le
Tableau 1 illustre la répartition des cas suspects de fièvre jaune par tranches d´âges au Togo de 2004-2014. Les enfants de 0-15 ans étaient les plus nombreux. La majorité des cas suspects (83,3%) avaient moins de 30 ans. La médiane d´âge des cas suspects était de 14 ans IIQ (6,5-25,5 ans). Le sexe ratio homme-femme (H/F) était de 3/2.
Cas probables
Sur les 3054 cas suspects notifiés, 33 personnes avaient des IgM positifs ils étaient majoritairement de sexe masculin 53,13%. L´âge médian des cas probables était de 16 ans IIQ (9-20 ans).
Cas confirmés
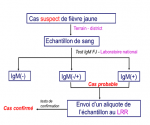
Les
Figure 2 et
Figure 3montrent la notification des cas et les cas confirmés en fonction des années et des districts. La plupart des cas confirmés (10/12) se trouve dans la partie nord du Togo. Le Togo a connu trois épidémies entre 2004 et 2014.
L´âge médian des cas confirmés était de 17,5 ans IIQ (9-26,5 ans).
Parmi les cas confirmés, 04 étaient des femmes soit un sexe ratio H/F de 2/1.
Réactivité du système de surveillance de la fièvre jaune au Togo
Environs 93,01 % (2833) des cas suspects ont été prélevés dans les 14 jours qui ont suivi le début des symptômes. La médiane du délai d´acheminement du district au laboratoire était de 5 jours IIQ (3-8 jours).
Un total de 28,39% des échantillons ont été acheminés dans les 72 heures après leur prélèvement au laboratoire.
Au total 99,54% des échantillons étaient arrivés dans de bonnes conditions au LNR.
La médiane du délai de rendu des résultats par le Laboratoire National de Référence après réception des échantillons était de 5 jours IIQ (2-7). Environs 77,95% des échantillons ont été manipulés par le LNR dans les 7 jours après leur prélèvement.
Le délai médian de confirmation par le LRR médian était de 17 jours IIQ (12-24jours).
Discussion


De 2004-2014, un total de 3054 de cas suspects ont été notifiés dont 33 ont été déclarés cas probables par le laboratoire national de référence et 12 cas ont été confirmés par le LRR.
La plupart des districts sanitaires du Togo (35/40) avait rapporté au moins un cas suspect par an. Quatre districts n´ont pas rapporté chaque année au moins un cas comme le recommande l´OMS, en effet se sont de nouveaux districts qui avaient été créés.
Les districts de l´Oti et de Tône ont enregistré le plus grand nombre de cas. Ces districts sont fronta-liers avec le Benin et le Ghana pour l´Oti puis le Ghana et le Burkina Faso pour Tône. En 2012 cer-tains districts du Ghana étaient rentrés en épidémie avant ceux du Togo [
3]. Ces districts sont dans un climat de type soudanien, l´écosystème se prête à la survie et à la multiplication des vecteurs :
Aedès [
10].
De 2005 à 2007 il n´y a pas eu de cas suspects manipulés au laboratoire national de référence mais la surveillance épidémiologique a continué et la confirmation biologique se faisait à Dakar sans que la base de données du laboratoire national ne soient actualisées. Les évaluations externes de qualité ne marchant pas au LNR, le laboratoire régional de Dakar traitait les échantillons directement et rem-plissait leur base de données.
Environs 93,01 % des cas suspects ont été prélevés dans les 14 jours qui ont suivi le début de la mala-die ce qui est conforme aux recommandations de l´OMS (> 80%) [
11]. L´OMS avait rapporté égale-ment pour le Togo en 2011 que 92,4% des cas suspects avaient été prélevés dans les 14 jours contre 93,2% pour le Burkina et 86,5% pour le Ghana [
12].
Le délai médian d´acheminement était de 5 jours mais seulement 28,39% arrivaient au laboratoire dans les 03jours alors que l´OMS recommande au moins 80%. Ceci est meilleur aux constats faits par l´OMS pour le Togo en 2011 où seulement 22 ,2% des échantillons étaient acheminés au LNR dans les 03 jours [
12]. La plupart des pays africains avaient également de faibles performances : 9,2% pour le Burkina et 41,4% pour le Ghana mais 94,5% pour le Benin [
12]. Ceci s´explique par le fait qu´il n´existe pas de moyen de transport consacré au convoyage des échantillons vers le laboratoire national de référence.
Le laboratoire mettait 5 jours pour manipuler les échantillons et 77,95% des résultats ont été rendus dans les 7 jours. Les performances du LNR sont inférieures aux 80% recommandés par l´OMS [
11]. Il y a eu une amélioration par rapport à l´année 2011 au cours de laquelle seulement 69,1% des échantil-lons étaient manipulés dans les 7 jours. Il en était pareil dans la plupart des pays de la région africaine de l´OMS [
12].
Le système de surveillance de la fièvre jaune du Togo met 17 jours pour détecter un cas suspect, le prélever et le confirmer au LNR. La fièvre jaune étant une maladie dont l´évolution peut conduire au décès dans la quinzaine jours après le début de la maladie [
1], en cas d´épidémie le système ne posera le diagnostic souvent en post mortem. Le système est peu réactif au vu de ce long délai de confirma-tion.
Limites
La principale limite de notre étude était son caractère rétrospectif. Nous n´avons pas interrogé les acteurs de la surveillance de la fièvre jaune au Togo. Néanmoins, cette étude nous a permis de contri-buer à décrire le système de surveillance de la fièvre jaune du Togo et à évaluer la simplicité, la repré-sentativité et la réactivité de ce système.
Conclusion


De 2004 à 2014, le système de surveillance de la fièvre jaune au Togo a détecté trois épidémies. Les sujets de moins de 20 ans ont été les plus atteints et les districts sanitaires ayant noté le plus grand nombre de cas étaient Tône et l´Oti.
Le système surveillance bien que représentatif est complexe et peu réactif du fait du long délai de confirmation biologique. Ce long délai de confirmation pourrait retarder la riposte en cas d´épidémie.
Nous suggérons la mise en place d´un système de convoyage rapide des échantillons au LNR.
Etat des connaissances actuelle sur le sujet
- La fièvre jaune est une fièvre virale hémorragique dont la létalité va de 50% à 80%
- Les vecteurs, les moustiques vivent sous des climats chauds et humides
- Plusieurs pays d’Afrique dont le Togo sont des pays où la fièvre jaune reste endémique
- La confirmation d’un cas suspect de fièvre jaune nécessite plusieurs étapes de confirmation biologique
Contribution de notre étude à la connaissance
- d’avoir une idée du délai entre les prélèvements de cas suspects et la confirmation au labora-toire
- d’apprenhender dans quelle mesure les méthodes complexes de confirmation impactent la ri-poste contre une épidémie de fièvre jaune au Togo
Conflits d'intérêts


Les auteurs ne déclarent aucun conflit d’intérêt.
Contributions des auteurs


WAH: a conçu le protocole, analysé la base de données, rédigé et finalisé l’article. AP: a contribué à la rédaction et à la finalisation de l’article. SAA, ANM, AMT : ont contribué à la finalisation de l’article. Y L, AYS, AK, KA: ont contribué à la saisie à l’analyse et à l’interprétation des résultats. CSN: a été le superviseur de la collecte des données sur le terrain. BS SNA: ont contribué à la rédaction du proto-cole et de l’article en faisant des commentaires. KB: a été le superviseur de la collecte des données sur le terrain et a contribué à la finalisation de l’article. Tous les auteurs ont lu et approuvé le manuscrit final.
Remerciements


Nos remerciements vont: Au Ministère de la Santé et de la Protection Sociale du Togo. A la Direction de Lutte contre les Maladies du Togo. A l’Institut National d’Hygiène de Lomé. Au Programme de Formation en Epidémiologie et Laboratoire de terrain du Burkina Faso Ouagadougou
Tableaux et figures


Tableau 1: Répartition des cas suspects de fièvre jaune en fonction des tranches d´âge
Figure 1: Répartition des cas suspects de Fièvre Jaune en fonction du temps au Togo , 2004-2014
Figure 2: Courbe épidémique de la fièvre jaune au Togo, 2004-2014
Figure 3: Répartition des confirmés de Fièvre Jaune par District au Togo, 2004-2014
Références


- Monath TP, Vasconcelos PF. Yellow fever. Journal of clinical virology. 2015 Mar 1; 64:160-73.https://doi.org/10.1016/j.jcv.2014.08.030 . Google Scholar
- Dussart P, Cesaire R, Sall A. Dengue, fièvre jaune et autres arboviroses. EMC - Maladies in-fectieuses. 2012 Apr; 9(2):1-24.http://dx.doi.org/10.1016/S1166-8598(12)50186-9
- Rogers DJ, Wilson AJ, Hay SI, Graham AJ. The Global Distribution of Yellow Fever and Dengue. Adv Parasitol. 2006; 62:181-220.https://doi.org/10.1016/S0065-308X(05)62006-4 Google Scholar
- World Health Organization. Yellow fe-ver fact sheet N° 100. WHO. Accessed 30 January 2019.
-
Jean K, Hamlet A, Benzler J, Cibrelus L, Gaythorpe KAM, Sall A, Ferguson NM, Garske T. Eliminating yellow fever epidemics in Africa: Vaccine demand forecast and impact modelling. PLOS Neglected Tropical Diseases. 2020 May 7; 14(5):e0008304.https://doi.org/10.1371/journal.pntd.0008304 PubMed | Google Scholar
-
Garske T, Van Kerkhove MD, Yactayo S, Ronveaux O, Lewis RF, Staples JE, Perea W, Ferguson NM, for the Yellow Fever Expert Committee. Yellow Fever in Africa: estimating the burden of disease and impact of mass vaccination from outbreak and serological data. PLoS Med. 2014 May; 11(5):e1001638.https://doi.org/10.1371/journal.pmed.1001638 PubMed | Google Scholar
- World Health Organization. Yellow fever surveillance and outbreak response: revision of case definitions, October 2010. Weekly Epidemiological Record= Relevé épidémiologique hebdo-madaire. 2010;85(47):465-72. Google Scholar
- Centers for Disease Control and Prevention. Guidelines for Evaluating Surveillance Systems. CDC. 198 Accessed Feb 2020. Google Scholar
- Togo, Ministère de la Santé. Surveillance Intégrée des Maladies et Riposte, Guide Technique, Togo : Edition 2010. Togo: MS; 2010. 366 p.
- Weaver SC, Reisen WK. Present and future arboviral threats. Antiviral Res. 2010 Feb; 85(2):328-45.https://doi.org/10.1016/j.antiviral.2009.10.008 PubMed | Google Scholar
- Organisation mondiale de la Santé (OMS - AFRO). Surveillance épidémiologique de la Fièvre Jaune dans la Région Africaine de l´OMS. Manuel pour le personnel de santé des pays participant au réseau de surveillance. Brazzaville, Congo: OMS-AFRO; Mai 2012. 42 p.
- WHO Africa Region. Epidemiology of Yellow Fever in the Africa region. Brazzaville, Congo: WHO- AFRO; 2011. 7 p.